Brasil
VACINA
Sputnik V: Reunião com Anvisa termina sem pedido de uso emergencial
Publicado: 21/01/2021 às 19:19
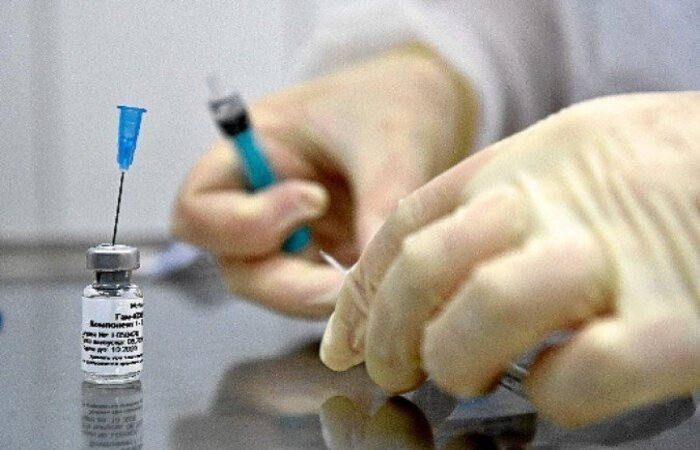
(Foto: Natalia Kolesnikova/AFP)
“Durante a reunião, os representantes da União Química afirmaram que estão interessados em cumprir todas as etapas regulatórias exigidas pela Anvisa para avançar com os estudos clínicos no Brasil”, explicou a agência. A Anvisa informou, também, que uma nova reunião de caráter técnico deve ser realizada para avançar no processo da vacina, mas não informou datas.
A União Química e o Fundo de Investimentos Diretos da Rússia (RDIF) protocolaram na última sexta-feira (15) um pedido emergencial junto à Anvisa, no entanto, a agência reguladora recusou os documentos já que a vacina Sputnik V não apresenta requisitos mínimos para realizar o pedido de uso emergencial.
Para solicitar esse tipo de autorização, a Anvisa pede que o imunizante tenha estudos de fase 3 no Brasil.Em entrevista ao Correio nesta quinta-feira, o diretor de Negócios da União Química disse que o Brasil já tem produção própria da Sputnik V e poderá ofertar doses, a depender da liberação da agência regulatória, em fevereiro. "A produção da vacina no Brasil é a autonomia que o país precisa para não depender do mercado internacional", afirmou.
10 milhões de doses
De acordo com ele, a ideia é conseguir autorização para importação de 10 milhões de doses prontas da Sputnik V. "O que queremos hoje, da Anvisa, é a aprovação emergencial para trazer 10 milhões de doses prontas da Rússia, a fim de atender rapidamente o mercado brasileiro diante dessa falta de vacina", pontuou Rosso.
Caso não haja liberação por parte da Anvisa, a União Química já negocia a exportação das produções nacionais para países da América do Sul que já aprovaram o uso emergencial da Sputnik V. Neste contexto, seriam beneficiados países com Argentina, Paraguai, Bolívia e Venezuela.
Últimas

Mais Lidas

